🔎 APPROFONDIMENTO: Finerenone
È il primo antagonista non steroideo del recettore mineralcorticoide indicato nella nefropatia diabetica. Efficacia modesta e costo elevato. [Lettura 7 min]
Nell’ottobre 2022, in Europa è stato approvato il finerenone, un antagonista dell'aldosterone indicato per il trattamento di pazienti adulti con nefropatia diabetica (stadio 3 e 4 con albuminuria).
A dicembre il Comitato per i Medicinali per Uso Umano (CHMP) dell'EMA ha raccomandato di estendere l'indicazione, togliendo la restrizione agli stadi 3 e 4.
Spironolattone (Aldactone°) ed eplerenone (Inspra°) sono antagonisti steroidei dei recettori mineralocorticoidi, indicati rispettivamente per iperaldosteronismo primario o secondario e ipertensione arteriosa e insufficienza cardiaca con ridotta frazione di eiezione.
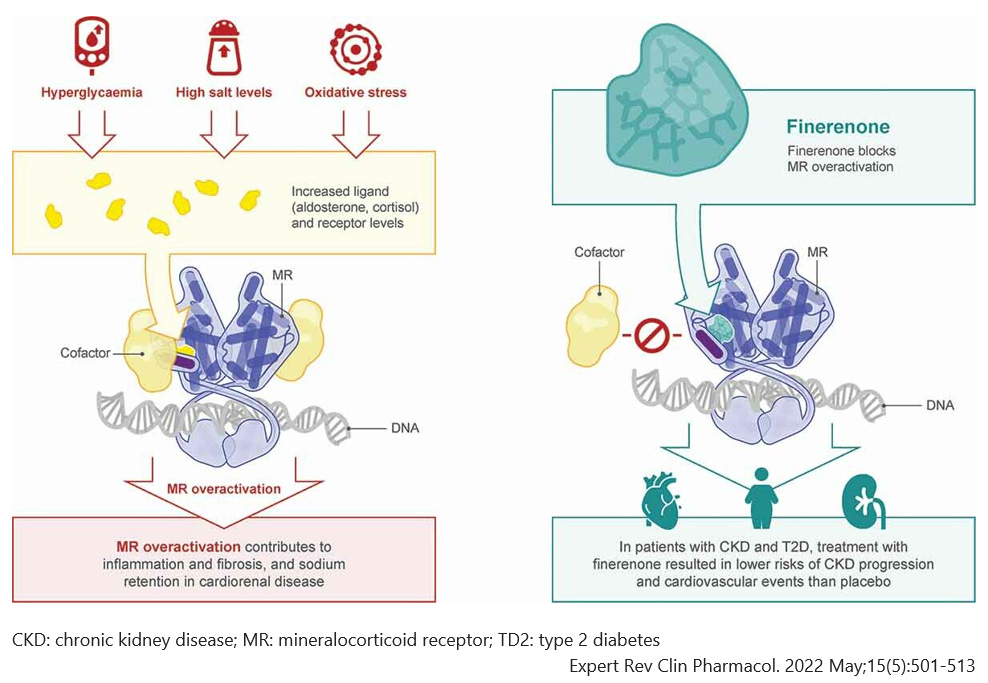
Il finerenone (Kerendia°) è un antagonista selettivo non steroideo dei recettori mineralcorticoidi: blocca il riassorbimento del sodio mediato da questi recettori e l'iperattivazione dei recettori stessi (presenti in rene, cuore e vasi) che potrebbe contribuire alla fibrosi e all'infiammazione.
Il finerenone ha una biodisponibilità del 43,5%, emivita 2-3 ore e viene eliminato per l’80% con le urine e il 20% con le feci.
Il metabolismo avviene prevalentemente attraverso il CYP3A4, con le prevedibili numerose interazioni con farmaci metabolizzati da questo isoenzima.
La posologia dipende dal valore di eGFR:
≥ 60: 20 mg
da ≥ 25 a < 60: 10 mg
< 25: non raccomandato
Efficacia
L’approvazione si è basata sullo studio randomizzato in doppio cieco FIDELIO-DKD, finanziato da Bayer, condotto su circa 5.700 adulti (70% uomini), età media 66 anni, con diabete di tipo 2 e malattia renale cronica con eGFR tra 25 e 75 ml/min, riduzione persistente moderata o grave del rapporto albumina-creatinina e potassiemia fino a 4,8 mmol/l.
Tutti i partecipanti seguivano una terapia standard che comprendeva la massima dose tollerata di un ACE-inibitore o di un sartano, come da linee guida.
I pazienti sono stati randomizzati a placebo o finerenone 10 mg o 20 mg (dose target) una volta al giorno, a seconda dell'eGFR e della potassiemia, con sospensione se necessario.
L'endpoint primario combinato era costituito da:
riduzione dell’eGFR almeno del 40% per almeno 4 settimane,
insufficienza renale (definita da almeno 4 settimane di riduzione dell’eGFR <15 ml/min, dialisi cronica o trapianto renale) e
morte per cause renali.
Nel corso del follow-up mediano di 2,6 anni, l’endpoint si è verificato nel 17,8% dei pazienti trattati con finerenone rispetto al 21,1% di quelli che assumevano placebo (hazard ratio [HR] 0,82; number needed to treat [NNT] = 29 per 3 anni).
La differenza era in gran parte dovuta a una riduzione meno frequente dell'eGFR, mentre non vi erano differenze significative per le altre componenti dell'endpoint.
L'EMA classifica l'effetto del trattamento come relativamente modesto.
Il principale endpoint secondario era costituito da:
infarto miocardico non fatale,
ictus,
morte cardiovascolare e
ricovero per insufficienza cardiaca.
L’endpoint secondario si è verificato nel 13,0% dei pazienti trattati con finerenone rispetto al 14,8% con placebo (HR 0,86).
Bayer aveva inizialmente richiesto l'approvazione del finerenone anche con l’indicazione di riduzione della morbilità e mortalità cardiovascolare. Tuttavia, l'EMA ha ritenuto che l'effetto non sia stato dimostrato in modo convincente.
L'estensione dell'indicazione attualmente raccomandata si basa probabilmente sui risultati dello studio in doppio cieco FIGARO-DKD, progettato in modo simile al precedente.
Lo studio ha valutato 7.400+ pazienti (69% uomini), età media 64 anni, con diabete di tipo 2 e malattia renale cronica.
I pazienti dovevano avere un rapporto albumina-creatinina moderatamente aumentato con eGFR compreso tra 25 e 90 ml/min (46% dei partecipanti) o un rapporto albumina-creatinina fortemente aumentato con eGFR di almeno 60 ml/ min.
Gli endpoint primari e secondari principali erano simili a quelli dello studio FIDELIO-DKD.
Dopo un follow-up mediano di 3,4 anni, l'endpoint primario si è verificato nel 12,4% con finerenone rispetto al 14,2% con il placebo (HR 0,87; NNT 47 per 3,5 anni).
Il beneficio in questo caso era dovuto principalmente alla riduzione dei ricoveri ospedalieri per insufficienza cardiaca (3,2% vs. 4,4%), unica componente dell'endpoint con una superiorità significativa.
Eventi avversi
A causa del meccanismo d'azione, il finerenone causa molto frequentemente iperkaliemia, spesso anche grave e nello studio FIDELIO ha causato la sospensione permanente della terapia nel 2,3% dei casi.
La funzione renale e la potassiemia vanno monitorate prima e durante il trattamento e può essere necessario ridurre il dosaggio del finerenone o sospenderlo.
La scheda tecnica italiana specifica che il trattamento non va iniziato con una potassiemia ≥5 mmol/l e durante il trattamento questo va sospeso se la potassiemia è >5,5 mmol/l.
Altri effetti avversi segnalati in scheda tecnica sono ipotensione, iponatriemia, iperuricemia, riduzione dell’eGFR, prurito e anemia.
Negli studi registrativi l'eGFR è diminuito in media di 2,4 ml/min rispetto al placebo e nei primi 24 mesi è risultato inferiore con il finerenone rispetto al placebo.
Negli studi sugli animali finerenone ha mostrato una tossicità riproduttiva. Da scheda tecnica, “non deve essere usato durante la gravidanza salvo dopo attenta valutazione del beneficio per la madre e del rischio per il feto”.
Le donne in età fertile devono usare misure contraccettive efficaci durante il trattamento.
La terapia con finerenone è controindicata in associazione a potenti inibitori del CYP3A4, come itraconazolo, ketoconazolo, ritonavir, nelfinavir, cobicistat, claritromicina, telitromicina, nefazodone, e nei pazienti con morbo di Addison.
Durante il trattamento va anche evitato il consumo di pompelmo o succo di pompelmo.
In pratica - I commentatori della rivista indipendente arznei-telegramm ritengono che non sia stato chiarito a sufficienza se finerenone abbia un effetto rilevante sugli endpoint renali e cardiovascolari, specifico del principio attivo e indipendente dalla riduzione della pressione arteriosa.
Inoltre, il beneficio in associazione o in confronto agli inibitori SGLT-2 non è chiaro.
La loro conclusione è che, allo stato attuale delle conoscenze, non c’è un'indicazione sicura per l'uso del finerenone.
La linea guida internazionale KDIGO formula solo una raccomandazione debole (2A) per l’utilizzo del finerenone nel diabete di tipo 2, in pazienti con eGFR ≥25 ml/min, potassiemia normale e rapporto albumina-creatinina ≥30 mg/g nonostante la massima dose tollerata di un inibitore del sistema renina-angiotensina.
Per ridurre il rischio di iperkaliemia, i pazienti dovrebbero avere livelli basali di potassiemia costantemente normali.
Gli autori sottolineano le incertezze relative al beneficio dell’associazione con inibitori SGLT-2, per i quali la linea guida formula una raccomandazione forte nei pazienti con diabete, malattia renale cronica ed eGFR di almeno 20 ml/min.
Gli esperti di UpToDate formulano una raccomandazione debole (2B) all’uso del finerenone in pazienti con le stesse caratteristiche, trattati con inibitore del sistema renina-angiotensina e inibitore SGLT-2.
Mancano, tuttavia, confronti diretti tra finerenone e inibitori SGLT-2, così come mancano studi randomizzati che verifichino se gli effetti sono additivi.
Nei due studi citati solo il 5% e l'8% dei pazienti assumeva un inibitore SGLT-2 al basale.
Costo: il trattamento con finerenone 10 mg o 20 mg ha un costo di circa 1600 €/anno (Kerendia° 28 compresse, 10 e 20 mg, € 123,21).
Finerenone: a mineralocorticoid receptor antagonist for the treatment of chronic kidney disease associated with type 2 diabetes.
Expert Rev Clin Pharmacol. 2022 May;15(5):501-513
Effect of Finerenone on Chronic Kidney Disease Outcomes in Type 2 Diabetes.
N Engl J Med. 2020 Dec 3;383(23):2219-2229
Cardiovascular Events with Finerenone in Kidney Disease and Type 2 Diabetes.
N Engl J Med. 2021 Dec 9;385(24):2252-2263
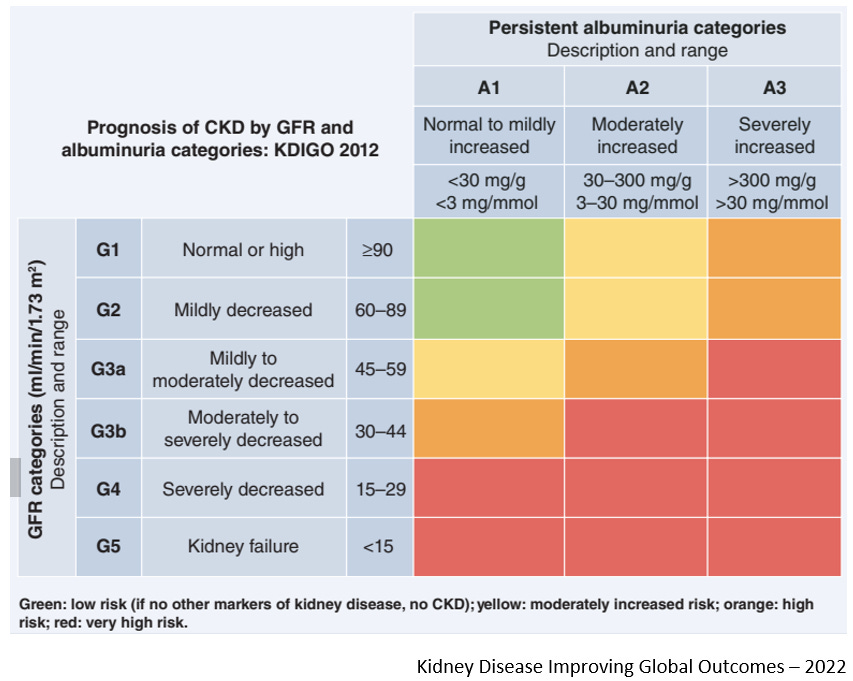
KDIGO 2022 Clinical Practice Guideline for Diabetes Management in Chronic Kidney Disease
Kidney Disease Improving Global Outcomes – 2022
Finerenon (Kerendia) bei diabetischer nephropathie
a-t 2023; 54: 3-5
Assessment report – Kerendia
EMA – 16/12/2021
Treatment of diabetic kidney disease
UpToDate - topic last updated: Jul 17, 2023
Gilberto Lacchia - Pubblicato: 30/09/2023 Aggiornato: 30/10/2023